Полногеномная полигенная оценка риска диабетической болезни почек при СД2
Исследователи: Ха Май Т. Ви, Серхио Деллепиан, Кумардип Чаудхари, Александр Блэр, Бенджамин С. Гликсберг, Стивен Г. Кока, Лили Чан, Джон Цицзян Хе, Рон До, Гириш Н. Надкарни
Продолжаем серию публикаций для медицинских экспертов — переводы препринтов актуальных медицинских статей и исследований, которых еще нет на русском языке. Представляем итоги исследования группы американских ученых, посвященного полногеномному моделированию риска диабетической болезни почек.
Ученые разработали полигенный подход, который позволил доказать необходимость включения вкладов двух показателей — соотношения альбумина и креатинина в моче и общей скорости клубочковой фильтрации для прогнозирования риска диабетической болезни почек.
|
Основные сокращения статьи: ДБП — диабетическая болезнь почек; |
Резюме: почему комплексное исследование лучше одиночной модели
Диабетическая болезнь почек (ДБП) рассматривается как частично наследственное заболевание, однако генетические факторы, лежащие в основе данной патологии, остаются по большей части неизвестными. Основная сложность для понимания данных факторов проистекает из гетерогенности и, вероятно, полигенности этиологии ДБП. Протеинурическая и непротеинурическая диабетическая болезнь почек определяются высоким соотношением альбумина/креатинина в моче (САКМ) и низкой оценочной скоростью клубочковой фильтрации (ОСКФ) креатинина.
В своем исследовании ученые стремились объединить сводные статистические данные по ОСКФ и САКМ, полученные в результате предыдущих полногеномных исследований ассоциаций, в одну прогностическую модель и связать ее с распространенностью ДБП. Для этого они провели соответствующие исследования, используя генетические данные 18 841 человека с диагнозом диабет 2-го типа, взятые в Биобанке Великобритании. В результате получилось вычислить две полногеномные полигенные степени риска (ПГПР), объединяющие эффекты общих вариантов, связанных с двумя результатами измерений, ОСКФ и САКМ.
Обнаружилось, что включение обоих полногеномных полигенных степеней риска в единую модель обеспечивает значительное улучшение по сравнению с использованием одиночной модели ПГПР, созданной на основе сводной статистики ПГИА для ДБП.
Также был проведен анализ репликации с использованием образцов, взятых у 5389 человек и хранящихся в мультиэтническом биобанке БайоМе. Выяснилось, что самые низкие показатели были у лиц африканского происхождения (несмотря на то, что комбинированная модель имела последовательное направление ассоциации). Соответственно, следует предпринять усилия для разработки и проверки полигенных подходов для различных популяций пациентов.
|
Таким образом доказано, что комплексное моделирование полигенных ассоциаций ОСКФ и САКМ связано с диабетической болезнью почек в большей степени, чем индивидуальное моделирование и модель ПГПР, включающая исключительно сводную статистику ДБП. Данное моделирование может использоваться для получения информации о биологии и прогрессировании. |
Методы исследования
При использовании результатов двух недавних полногеномных исследований ассоциаций (ПГИА) для двух фенотипов — ОСКФ и САКМ, были получены две независимые полногеномные полигенные степени риска (ПГПР). Затем модель для прогнозирования диабетической болезни почек, включающая две степени ПГПР, была протестирована с использованием генетических данных 18 841 человека с диагнозом диабет 2-го типа, взятых в Биобанке Великобритании, и впоследствии проверена для других этнических групп с использованием образцов из биобанка БайоМе.
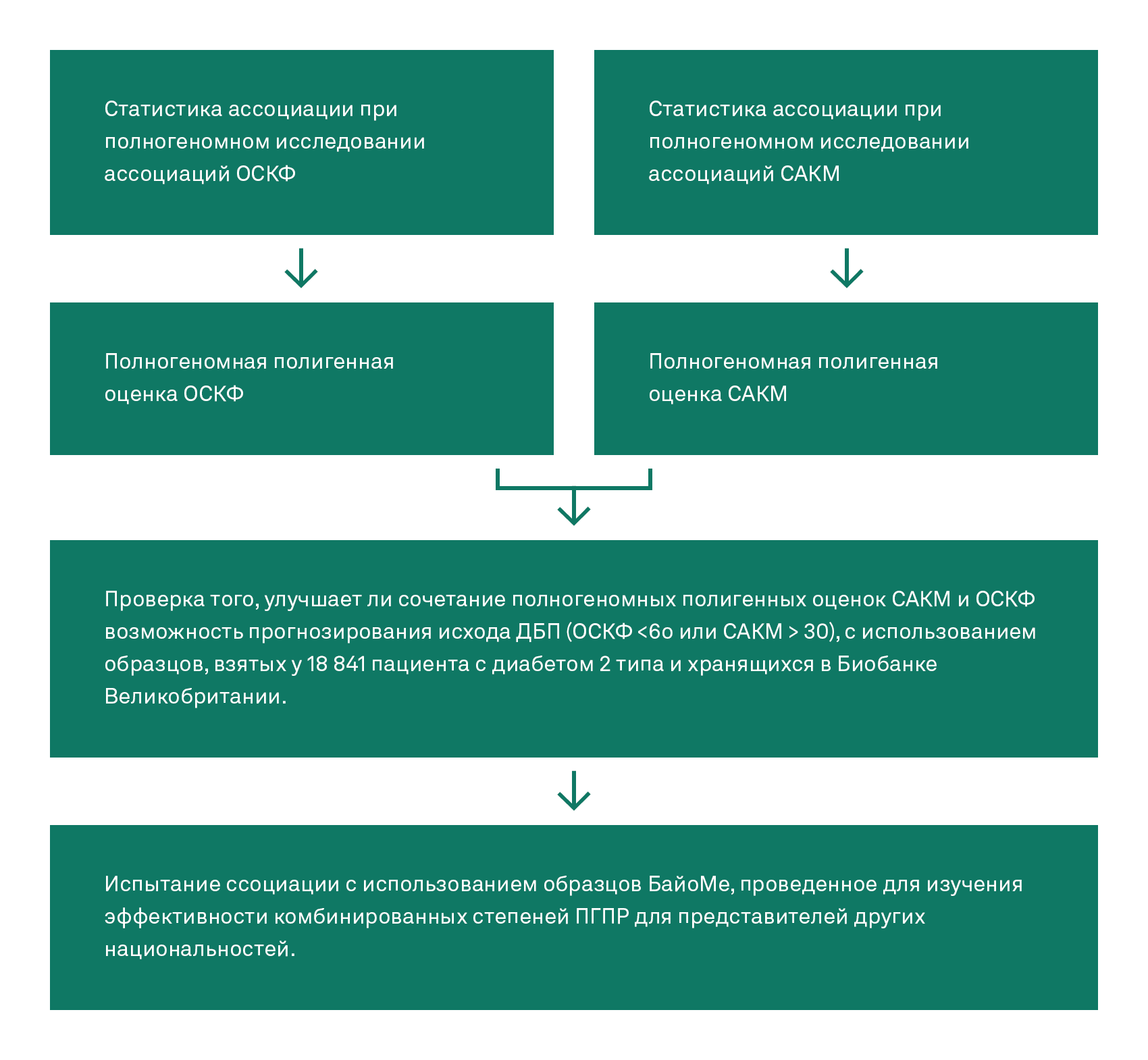
Описание когорт
Биобанк Великобритании является ресурсом для проведения масштабного проспективного популяционного когортного исследования, в котором приняли участие около 500 000 человек в возрасте от 39 до 73 лет, набранных в 22 оценочных центрах Великобритании в период с 2006 по 2010 год.(17,18)
Биобанк БайоМе представляет собой когорту медицинских биобанков, связанных с электронным медицинским архивом и включающих более чем 45 000 образцов, взятых у людей различного происхождения (включая африканское, латиноамериканское и европейское), с сопутствующими полногеномными данными генотипирования для 32 595 участников. Наряду с генетической информацией, биобанк БайоМе связан с широким спектром биомедицинских характеристик, поступающих из общесистемного электронного медицинского архива (ЭМА) Mount Sinai.
Идентификация состояния: случай / контроль Д2Т
Статистический анализ, проведенный в рамках данного исследования, был ограничен пациентами с диабетом 2-го типа (Д2Т). В Биобанке Великобритании пациентов с Д2Т определяли с помощью кодов Международной классификации болезней (ICD-9 250.00, 250.10; ICD-10 E11), либо с помощью кодов заболеваний (1223), сообщаемых самими пациентами, посредством устного интервью. В биобанке БайоМе пациентов с Д2Т определяли на основе алгоритма выбора случая и контроля, разработанного консорциумом eMERGE, который учитывает коды Международной классификации болезней для Д1Т и Д2Т, а также лабораторные показатели и диагнозы, поставленные врачами.
Статистический анализ
a. Генерация степеней ПГПР (полногеномные полигенные степени риска).
Степень ПГПР используется для оценки совокупного воздействия распространенных вариантов на риск возникновения определенных расстройств или заболеваний. Мы полагаем, что влияние независимых вариантов оказывает аддитивный эффект.
b. Испытания степеней ПГПР.
Ассоциации между протеинурической ДБП, непротеинурической ДБП и соответствующими степенями ПГПР были испытаны с использованием простой регрессионной логистической модели, скорректированной с учетом возраста, пола, центра оценки, партии измерения генотипа и первых десяти основных генетических компонентов (ОГК). Для каждого фенотипа было девять степеней ПГПР, из которых для последующего анализа были выбраны показатели с наиболее сильным отношением рисков и соответствующим наименьшим P-значением.
c. Ассоциация ПГПР оценочной скорости клубочковой фильтрации и ПГПР соотношения альбумина/креатинина в моче с комбинированным случаем ДБП.
Комбинированные случаи ДБП определялись как пациенты с ОСКФ <60 мл/мин / 1,73 м2 и/или САКМ ≥ 30 мг/г. Ассоциации между комбинированными случаями ДБП и степенями ПГПР были испытаны с использованием модели одиночных полигенных показателей, которая была отдельно испытана для каждой степени ПГПР, и модели множественных полигенных показателей, которые объединили два полигенных показателя в одну регрессионную логистическую модель. Ковариаты включали возраст, пол, ИМТ, систолическое артериальное давление (САД), центр оценки, партию образцов для измерения генотипа и первые 10 ОГК.
d. Валидация в нескольких этнических группах.
Два полногеномных полигенных показателя, ПГПР ОСКФ и ПГПР САКМ, были сгенерированы для каждого пациента, включенного в набор данных биобанка БайоМе. Затем ассоциации между степенью ПГПР и комбинированными случаями ДБП были испытаны в когортах американцев европейского происхождения, американцев латиноамериканского происхождения и афроамериканцев (по отдельности) с использованием модели множественных полигенных показателей, скорректированной с учетом возраста, пола, систолического артериального давления, ИМТ и первых десяти ОГК.
Общие результаты исследования
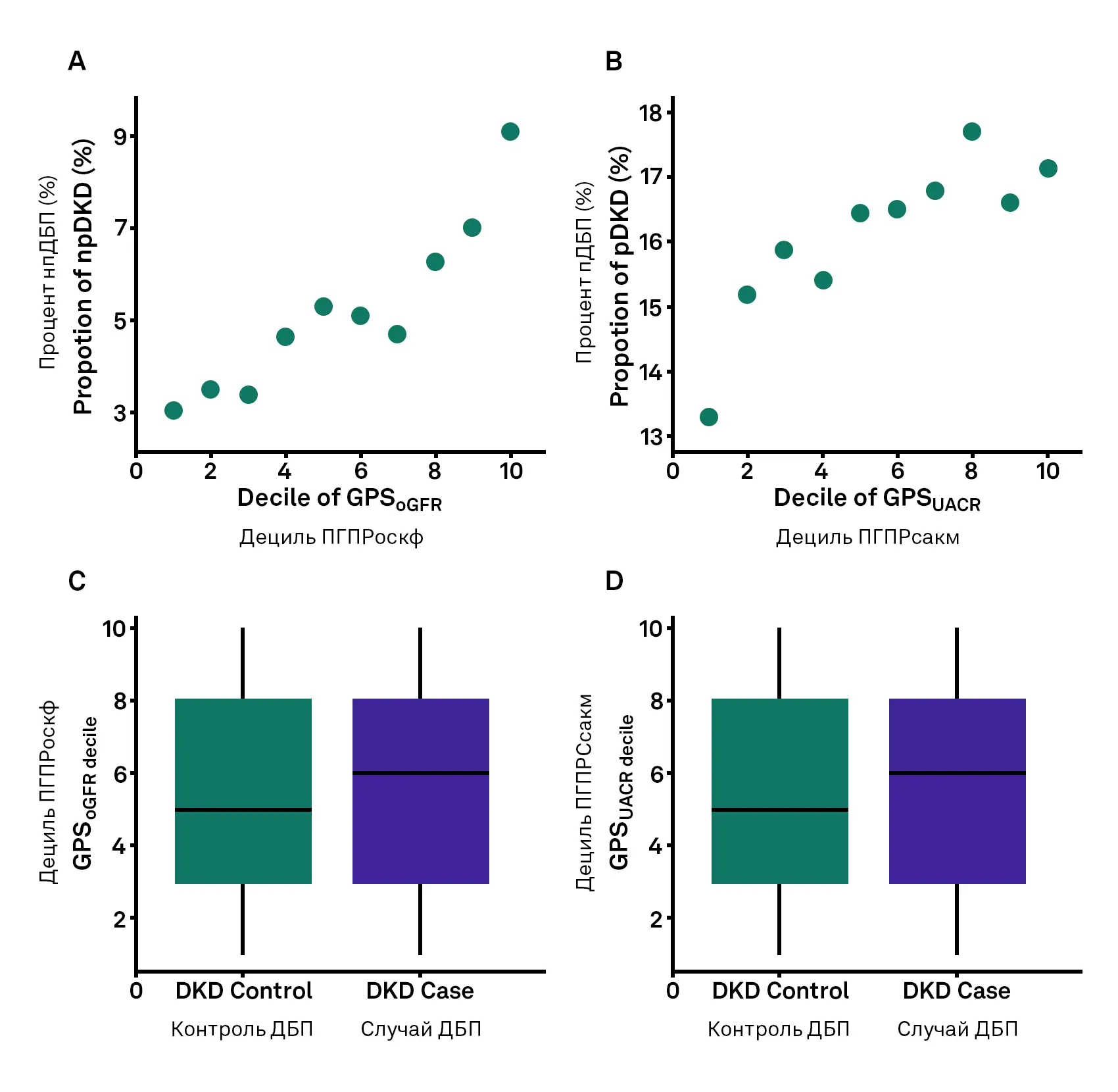
Ассоциация с распространением ДБП увеличивается параллельно с увеличением полногеномных полигенных показателей.
Верхний ряд: доля инцидентов ДБП в каждом дециле ПГПР. нпДБП определяется как ОСКФ < 6060 мл/мин / 1,73 м2 (A); пДБП определяется как САКМ <30 мг/г (B).
Нижний ряд: дециль ПГПР среди случаев ДБП по сравнению с контрольной группой. На каждой коробчатой диаграмме показан диапазон децилей от первого до третьего квартиля, а горизонтальная линия в середине указывает среднее децильное значение.
|
|
|
|
| Из 18 841 пациента с диабетом второго типа, включенных в Биобанк Великобритании, у 3498 пациентов (20%) наблюдалась диабетическая болезнь почек (ДБП). | У пациентов с ДБП в 781 случае наблюдалась почечная дисфункция (ОСКФ < 60 мл/мин / 1,73 м2) без протеинурии (САКМ < 30 мг/г), а в 2717 случаях наблюдалась протеинурия (САКМ ≥ 30 мг/г). | У пациентов с ДБП в среднем были более высокие показатели возраста, ИМТ и САД, чем у пациентов без ДБП. |
Показатели по каждой степени ПГПР
Полногеномная полигенная степень риска ОСКФ, соответствующая 1% причинных вариантов (ρ = 0,01), была лучшим прогностическим фактором нпДБП (p-значение = 3,33 × 10—26; R2 = 0,07).
Для пДБП, степень ПГПР САКМ, соответствующая 0,3% причинных вариантов (ρ = 0,003), показала лучшую эффективность (значение p = 1,8 × 10-4; R2 = 0,006). Поэтому мы выдвинули эти две степени ПГПР для включения в модель множественных полигенных показателей.
| Исследователи отметили, что увеличение степени ПГПР было связано с повышенным риском ДБП. Частота случаев ДБП увеличивалась пропорционально ПГПР ОСКФ и ПГПР САКМ, с увеличением нпДБП от самого низкого дециля до самого высокого дециля ПГПРОСКФ примерно на 7% и с увеличением пДБП от самого низкого дециля до самого высокого дециля ПГПРСАКМ примерно на 5%. Медиана децильной оценки степени ПГПР составила 6 для пациентов с ДБП по сравнению с 5 для пациентов без ДБП. |
Комплексное прогнозирование ПГПР ОСКФ и ПГПР САКМ
Несмотря на то, что две степени ПГПР независимы одна от другой, результаты испытания на логистическую регрессию с использованием модели множественной полигенной оценки показали сильную связь между степенями ПГПР и ДБП (p-значение 1,1 × 10-8 и 1,5 × 10−4 для ПГПР ОСКФ и ПГПР САКМ соответственно. Вклад каждой степени ПГПР в стратификацию риска ДБП был небольшим, о чем свидетельствует отношение рисков 1,13 для ПГПР ОСКФ и 1,08 для ПГПР САКМ.
| Однако по сравнению с одиночной моделью ПГПР, в которой используется степень ПГПР, полученная с помощью сводной статистики ПГИА для ДБП, модель множественных показателей продемонстрировала значительное улучшение. |
Затем было проведено исследование с целью определения, существует ли какое-либо существенное клиническое различие между пациентами с высоким и с низким распределением экстремального значения полигенных показателей.
| Наблюдалось усиление ассоциации между более высокими полигенными показателями и ДБП по сравнению с пациентами, у которых были более низкие полигенные показатели. Наиболее яркие признаки ДБП наблюдались у 10% пациентов с наивысшими уровнями как ПГПР ОСКФ, так и ПГПР САКМ. У таких пациентов отмечался более чем двукратный скорректированный риск диагноза ДБП (отношение рисков 2,15, 95% ДИ 1,02-4,68; p=0,04). |
Показатели ПГПР ОСКФ и ПГПР САКМ у разных этнических групп
Проведена оценка эффективности модели множественных полигенных показателей в трех различных этнических группах с помощью следующих образцов, взятых в биобанке БайоМе: 1855 афроамериканцев (AA); 2684 американца латиноамериканского происхождения (АЛАП); и 850 американцев европейского происхождения.
| Испытания на логистическую регрессию между ДБП и степенями ПГПР показали только одну значимую ассоциацию между ДБП и ПГПР ОСКФ в группе американцев латиноамериканского происхождения. Возможно, данный результат обусловлен тем фактом, что группа АЛАП была с наибольшим размером выборки, тем не менее исследователи наблюдали устойчивое направление ассоциации (отношение рисков >1). | |
| Самый высокий уровень показателя R2 наблюдался в группе АЕП, а самый низкий — в группе AA, что является показателем того, что полученные значения степеней ПГПР демонстрируют лучшие результаты в европейских и смешанных европейских этнических группах. |
Итоги работы
В данном исследовании группа ученых разработала полигенный подход, который объединил генетическую информацию из двух полногеномных полигенных данных, включающих в себя два признака, определяющих диабетическую болезнь почек — САКМ — соотношение альбумина и креатинина в моче и ОСКФ — общую скорость клубочковой фильтрации.
Во-первых, было выявлено, что среди пациентов с Д2Т, образцы которых были взяты в ББВ, у лиц, которые были отнесены к верхним децилям двух ПГПР, наблюдалось более чем двукратное увеличение риска ДБП по сравнению с лицами, которые были отнесены к нижним децилям.
Во-вторых, обнаружено, что объединение информации как об ОСКФ, так и об САКМ, обеспечивает лучшую ассоциацию с ДБП по сравнению с использованием исключительно значимых совпадений ПГИА для ДБП.
Наконец, что производительность данного комплексного моделирования значительно ниже в группе афроамериканцев, чем в группе американцев европейского происхождения, что указывает на необходимость улучшения разнообразия в данных исследованиях.
Обсуждение
Вышеописанные исследования показали, что комбинация изменений ОСКФ и САКМ является лучшим прогностическим фактором серьезных почечных нарушений, чем когда данные изменения оцениваются по отдельности. (30) Также важно отметить, что объединение генетической информации из двух независимых степеней ПГПР для двух количественных признаков обеспечивает более сильную ассоциацию с ДБП, чем использование исключительно значимых полногеномных совпадений ПГИА для ДБП.
Было доказано, что риск развития ДБП частично связан с генетическими факторами, однако на данный момент еще мало изучен вопрос его генетической архитектуры. Несмотря на то, что были предприняты серьезные усилия для обнаружения вариантов и генов, оказывающих большое влияние на ДБП при диабете 1 или 2 типа, поступали сообщения только о нескольких вариантах без надежной статистической мощности или независимой проверки. (31)
Фактически, в результате исследований ПГИА для ОСКФ и САКМ было обнаружено, что некоторые значимые полногеномные варианты являются частью биологически интересных путей, которые включают, помимо всего прочего, гомеостаз глюкозы, регуляторную функцию в почках, снижение обратного захвата альбумина, снижение везикулярного транспорта альбумина и изменение белков клубочковой базальной мембраны. (32-35)
Более того, дисфункция почек при диабете может быть обусловлена не только первичным повреждением нефрона в результате гипергликемии, но и такими вторичными процессами, как старение и систолическое артериальное давление. Эти биологические пути сложны и включают тысячи сайтов ОНП, из чего можно сделать вывод, что будущее направление исследований ДБП должно быть сосредоточено на полигенной природе заболевания и изучении путей, регулируемых множеством аллелей.
Хотя отсутствие убедительных доказательств в пользу мутации и гена с большим эффектом объясняется небольшим количеством пациентов, принимавших участие в этих исследованиях, возникают предположения, что ДБП может быть полигенным заболеванием, а восприимчивость пациента может быть обусловлена суммарным эффектом многочисленных распространенных вариантов, которые по отдельности производят небольшой эффект.
Данное исследование служит доказательством того факта, что комплексное моделирование полигенных вкладов ОСКФ и САКМ может улучшить ассоциацию с ДБП. Оно подчеркивает полигенную природу ДБП и подтверждает, что генетическая информация, накопленная в степени ПГПР, является важным фактором для прогнозирования риска, который может быть включен в прогностические модели.
Источник: medRxiv*
*– Настоящая статья является предварительной публикацией (препринтом) и не рецензировалась. В ней содержатся данные новых медицинских исследований, которые подлежат оценке и поэтому не должны использоваться в клинической практике.